Redox Biology: 抑制鐵死亡促進實驗性視神經病變視網膜神經節細胞存活
視網膜神經節細胞(RGC)死亡是外傷性視神經病變、青光眼和其他導致不可逆性視力喪失的視神經疾病的標志。然而,挽救RGC丟失的治療策略仍然具有挑戰性,RGC丟失的分子機制尚未完全闡明。

圖片來源:https://doi.org/10.1016/j.redox.2022.102541
近日,來自天津醫科大學總醫院的研究者們在Redox Biology雜志上發表了題為“Inhibition of ferroptosis promotes retina ganglion cell survival in experimental optic neuropathies”的文章,該研究結果表明,在實驗性青光眼和ONC模型中,鐵死亡是RGC調節細胞死亡的一種主要形式,并提示靶向線粒體依賴性鐵死亡作為視神經病變中RGC損傷的保護策略。
在本研究中,研究者使用青光眼和視神經擠壓(ONC)的實驗模型,強調了鐵死亡在RGC死亡中的作用。鐵死亡是一種非凋亡性的程序性細胞死亡形式,其特征是鐵依賴的致死性過氧化脂質積聚。
ONC治療后大鼠視網膜谷胱甘肽過氧化物酶4(Gpx4)和XC系統半胱氨酸/谷氨酸逆向轉運體(Xct)表達顯著下調,同時脂質過氧化和鐵水平升高。激光捕獲顯微切割和聚合酶鏈式反應證實了視網膜神經節細胞中Gpx4表達的降低。
透射電子顯微鏡顯示視網膜神經節細胞線粒體形態發生改變,包括膜密度增加和線粒體脊減少。值得注意的是,在ONC和微珠誘導的青光眼小鼠模型中,鐵死亡抑制劑鐵蛋白-1(Fer-1)顯著促進了RGC的存活并保護了視網膜功能。此外,與細胞凋亡抑制劑Z-VAD-FMK相比,Fer-1在挽救ONC視網膜RGC死亡方面顯示出更好的效果。
從機制上講,研究者發現Gpx4的下調主要發生在線粒體室,并伴隨著線粒體活性氧(ROS)和過氧化脂質的增加。線粒體選擇性抗氧化劑MitoTEMPO減輕了ONC后RGC的丟失,提示線粒體ROS和脂質過氧化是鐵死亡誘導ONC視網膜RGC死亡的主要機制。值得注意的是,Fer-1有效地阻止了ONC視網膜線粒體過氧化脂質的產生,線粒體5‘-三磷酸(ATP)產生的損害,以及線粒體基因如mt-cytb和MT-ATP6的下調。
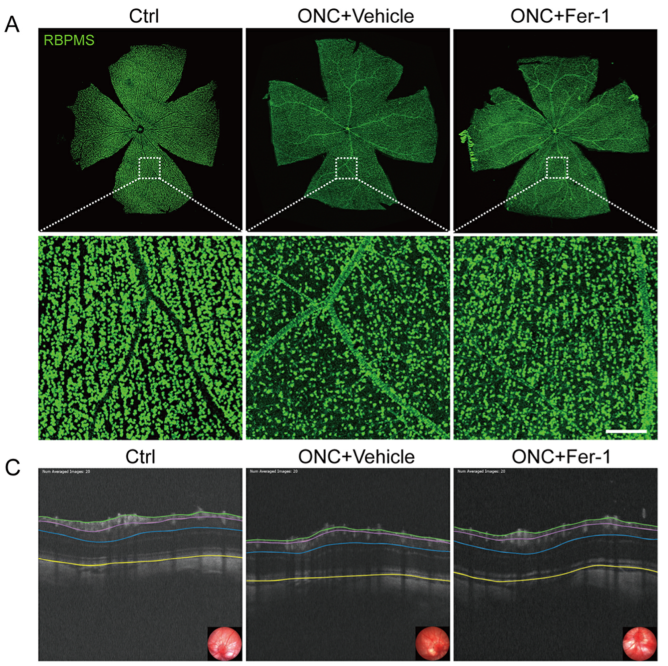
FER-1對ONC引起的RGC丟失、視網膜厚度減少和視網膜功能損害具有保護作用
圖片來源:https://doi.org/10.1016/j.redox.2022.102541
綜上所述,本研究揭示了線粒體依賴的鐵死亡介導視神經損傷后RGC死亡的新機制,可能為減少視神經疾病中RGC變性發現新的治療靶點。(Bioon.com)
參考文獻
Miao Guo et al. Inhibition of ferroptosis promotes retina ganglion cell survival in experimental optic neuropathies. Redox Biol. 2022 Dec;58:102541. doi: 10.1016/j.redox.2022.102541.

- 上一篇

Redox Biology : ESCC癌細胞如何利用代謝轉換形成遠處轉移提供了新的見解
轉移擴散通常會導致癌癥的致命后果。新出現的證據表明,只有原發癌細胞的亞群進行多步驟重新編程,以獲得侵蝕周圍環境和逃避循環中的細胞凋亡的能力,才能在遠處器官中形成轉移灶。 另一方面,所有使轉移細胞能夠應對細胞外壓力和陌生微環境的信號都可能構成癌癥治療的脆弱性。識別轉移網絡中的重要結節將提供新的機會,以改進抗癌治療,超越目前的策略,并在轉移過程中甚至轉移前消除結
- 下一篇
細胞在胚胎發生過程中構建組織時如何感知其機械環境
德累斯頓工業大學和加州大學圣巴巴拉分校卓越生命物理集群的一個研究小組揭示了細胞在胚胎發生過程中構建組織時如何感知其機械環境。構建組織和器官是細胞在胚胎發生過程中必須完成的最復雜和最基本的任務之一。在這項集體任務中,細胞通過各種交流方式進行交流,包括生化信號(類似于細胞的嗅覺)和機械信號(細胞的觸覺)。幾十年來,各種學科的研究人員一直對細胞通信著迷。Otger
