NEJM:KRAS抑制劑Adagrasib聯合或不聯合西妥昔單抗對結直腸癌的療效與安全性(KRYSTAL-1研究)
在30%~40%的結直腸癌會出現KRAS突變,作為靶向治療中的“釘子戶”一般的存在,近40年來,幾乎所有靶向藥都在KRAS基因突變的面前紛紛折戟。
根據醫學文獻所報道,KRAS是實體瘤中最常見的癌基因之一,大約30%的腫瘤都存在KRAS突變,包括90%的胰腺癌,30%~40%結直腸癌和15%~20%的肺癌。然而,KRAS靶向藥卻寥寥無幾,KRAS一度成為無藥可用的最難突變。
Adagrasib(MRTX849)是一款針對KRAS G12C突變體的特異性優化口服抑制劑,在非小細胞肺癌和結直腸癌及其他實體腫瘤治療中展現出良好的療效,成為繼Sotorasib之后第二款獲批上市的KRAS抑制劑。Adagrasib具有長達24小時的半衰期和廣泛的組織分布,而且能夠穿過血腦屏障,有助于最大限度地發揮藥物效力。
除了在非小細胞肺癌中,Adagrasib在KRAS G12C 突變晚期實體瘤患者中展現出驚人的療效。在2021年ESMO大會上報道了關于Adagrasib治療結直腸癌患者的初步研究結果,分為Adagrasib單藥治療組及Adagrasib聯合西妥昔單抗組。此次在最新的NEJM上完整報告KRYSTAL-1試驗結果。
同時,KRYSTAL-1試驗1b期隊列研究數據,2022年12月21日,Mirati Therapeutics(簡稱“Mirati”)宣布,FDA已授予adagrasib(KRAZATI)與西妥昔單抗(cetuximab)聯合用于 KRASG12C 突變晚期結直腸癌 (CRC) 患者的突破性治療指定(BTD),這些癌癥患者先前接受化療和抗 VEGF 治療之后出現疾病進展。
在這項 1-2 期、開放標簽、非隨機臨床試驗中,我們分配接受過大量預處理的 KRAS G12C 突變型轉移性結直腸癌患者接受Adagrasib單藥治療(600 毫克,每天兩次口服)或Adagrasib(相同劑量)與 每周一次靜脈注射西妥昔單抗(初始負荷劑量為每平方米體表面積 400 毫克,隨后劑量為每平方米 250 毫克)或每 2 周一次(劑量為每平方米 500 毫克)。 主要終點是客觀反應(完全或部分反應)和安全性。
結果顯示,截至 2022 年 6 月 16 日,共有 44 名患者接受了Adagrasib,32 名患者接受了Adagrasib和西妥昔單抗的聯合治療,中位隨訪時間分別為 20.1 個月和 17.5 個月。 在單藥治療組(43 名可評估患者)中,19% 的患者有客觀反應(95% 置信區間 [CI],8 至 33)。 中位反應持續時間為 4.3 個月(95% CI,2.3 至 8.3),中位無進展生存期為 5.6 個月(95% CI,4.1 至 8.3)。 在聯合治療組(28 名可評估患者)中,反應率為 46%(95% CI,28 至 66)。 中位反應持續時間為 7.6 個月(95% CI,5.7 至不可估計),中位無進展生存期為 6.9 個月(95% CI,5.4 至 8.1)。 單藥治療組 3 級或 4 級治療相關不良事件的百分比為 34%,聯合治療組為 16%。 未觀察到 5 級不良事件。
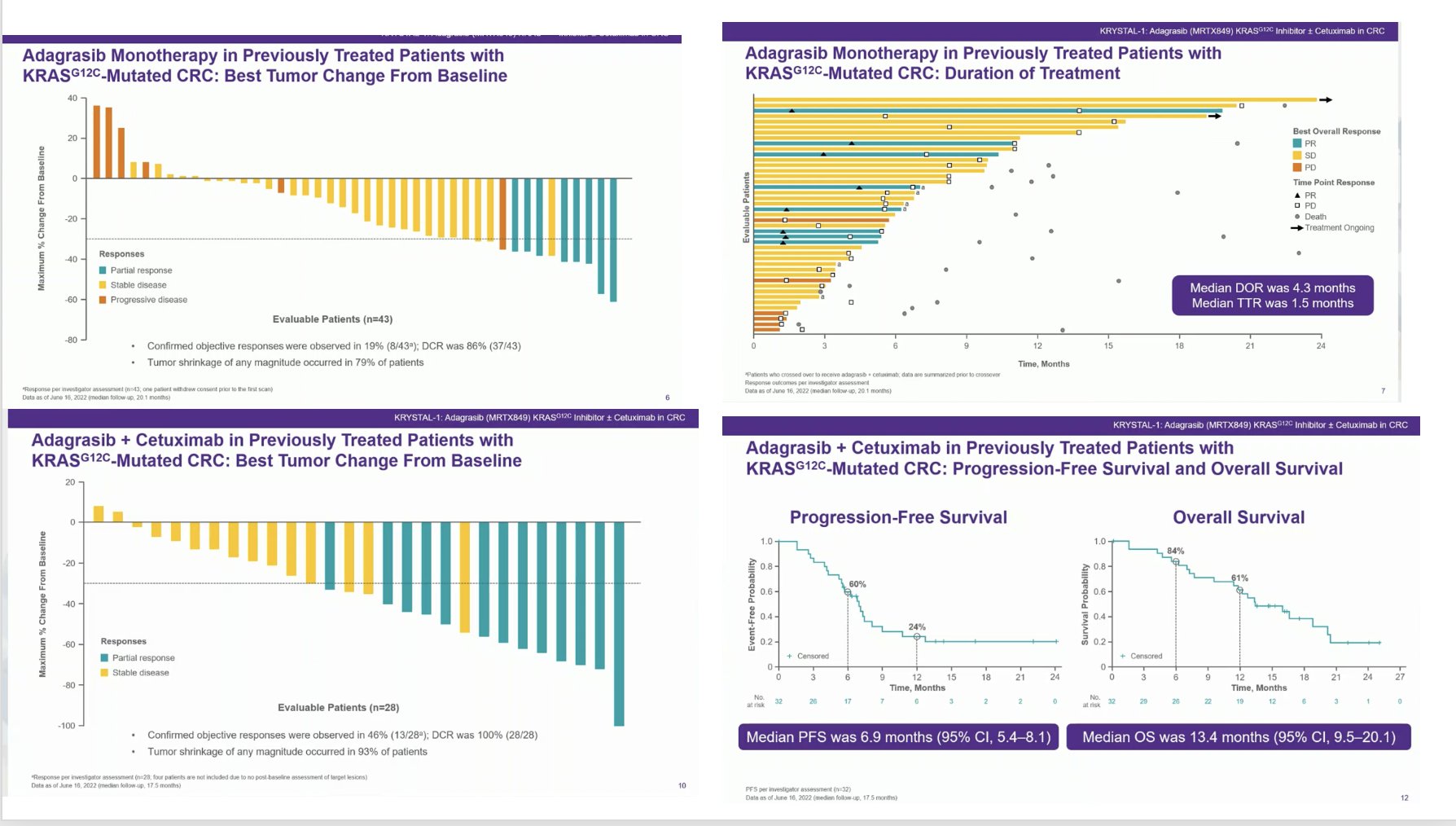
這些研究結果表明,Adagrasib 在經過大量預處理的 KRAS G12C 突變型轉移性結直腸癌患者中具有抗腫瘤活性,無論是作為口服單一療法還是與西妥昔單抗聯合使用。 聯合治療組的中位反應持續時間超過 6 個月。可逆性不良事件在兩組中都很常見。另外,Adagrasib與西妥昔單抗聯合治療,效果會更好。


