加州伯克利大學發現“病毒毒素”可導致重癥COVID-19
發表在《Nature Communications》雜志上的一項新研究揭示了SARS-CoV-2病毒產生的病毒毒素可能會導致嚴重的COVID-19感染。
這項研究顯示了部分SARS-CoV-2“刺突”蛋白如何破壞身體器官(如肺部)血管內部的細胞屏障,導致所謂的血管泄漏。阻斷這種蛋白質的活性可能有助于預防COVID-19的一些致命癥狀,包括肺水腫,肺水腫會導致急性呼吸窘迫綜合征(ARDS)。
“從理論上講,通過專門針對這一途徑,我們可以阻斷導致血管疾病和急性呼吸窘迫綜合征的發病機制,而不需要針對病毒本身,”該研究的主要作者、加州大學伯克利分校的博士后學者Scott B. Biering說。“鑒于所有正在出現的不同變體,以及單獨預防每種變體的感染的困難,除了完全阻止感染之外,關注這些致病的觸發因素可能是有益的。”
雖然許多疫苗懷疑人士對SARS-CoV-2刺突蛋白(COVID-19 mRNA疫苗的靶標)的潛在危險表示擔憂,但研究人員表示,他們的工作沒有提供證據表明,在沒有病毒感染的情況下,刺突蛋白會引起癥狀。相反,他們的研究表明,刺突蛋白可能與病毒和身體自身的免疫反應協同作用,引發危及生命的癥狀。
此外,接種疫苗后體內循環的刺突蛋白的濃度遠低于在嚴重COVID-19患者中觀察到的濃度和研究中使用的濃度。
該研究的資深作者、加州大學伯克利分校的傳染病和疫苗學教授Eva Harris說:“疫苗中含有的刺突蛋白的數量永遠不會導致泄漏。此外,沒有證據表明(刺突蛋白)本身具有致病性。我們的想法是,它能夠幫助和教唆持續的感染。”
通過研究SARS-CoV-2刺突蛋白對人類肺部和血管細胞以及小鼠肺部的影響,研究小組發現了允許刺突蛋白破壞體內關鍵屏障的分子途徑。除了為治療嚴重的COVID-19開辟新的途徑外,了解刺突蛋白是如何導致血管滲漏的,還可以揭示其他新興傳染病背后的病理學。
Biering說:“我們認為,許多導致嚴重疾病的病毒可能會編碼一種病毒毒素。這些蛋白質不受病毒感染,與屏障細胞相互作用,導致這些屏障失靈。這使得病毒得以傳播,病毒的放大和血管泄漏是引發嚴重疾病的原因。我希望我們可以利用我們從SARS-CoV-2病毒中學到的原理,找到阻斷這種發病機制的方法,以便在下一次大流行發生時做好更充分的準備。”
刺突蛋白如何引發血管滲漏
當排列在血管和毛細血管上的細胞被破壞,導致血漿和其他液體從血液中泄漏時,就會發生血管滲漏。除了在重癥COVID-19中觀察到的肺和心臟損傷外,血管滲漏還可導致低血容量性休克,這是登革熱死亡的主要原因。
在COVID-19大流行之前,Biering和Harris研究項目的其他成員正在研究登革熱病毒蛋白NS1在觸發血管滲漏和導致低血容量性休克中的作用。當大流行爆發時,該團隊想知道SARS-CoV-2中類似的病毒毒素是否也可能導致導致COVID-19患者死亡的急性呼吸窘迫綜合征。
Harris說:“人們已經意識到細菌毒素的作用,但病毒毒素的概念仍然是一個真正的新概念。”“我們已經確定了這種從登革病毒感染的細胞中分泌的蛋白質,即使在沒有病毒的情況下,也能夠引起內皮細胞的通透性并破壞內部屏障。所以,我們想知道SARS-CoV-2蛋白質,如spike,是否能夠做類似的事情。”
刺突蛋白覆蓋在SARS-CoV-2的外表面,使病毒具有多節的外觀。它們在幫助病毒感染宿主方面發揮著關鍵作用:刺突蛋白與人類和其他哺乳動物細胞上的一種名為ACE2的受體結合,就像鑰匙轉動鎖一樣,允許病毒進入細胞并劫持細胞功能。SARS-CoV-2病毒感染細胞時,會脫落大量含有受體結合結構域(RBD)的刺突蛋白。
Biering說:“真正有趣的是,循環刺突蛋白與臨床中嚴重的COVID-19病例相關。我們想知道這種蛋白質是否也導致了我們在SARS-CoV-2中看到的任何血管泄漏。”
目前,科學家將與嚴重的COVID-19相關的心肺損傷歸因于一種被稱為細胞因子風暴的過度活躍的免疫反應。為了驗證刺突蛋白可能也起作用的理論,Biering和其他團隊成員使用薄層的人體內皮細胞和上皮細胞來模擬體內血管的內襯。他們發現,將這些細胞層暴露在刺突蛋白下增加了它們的滲透性,這是血管滲漏的標志。
利用CRISPR-Cas9基因編輯技術,研究小組表明,即使在不表達ACE2受體的細胞中,滲透性也會增加,這表明它可以獨立于病毒感染而發生。此外,他們發現暴露于刺突蛋白的小鼠也表現出血管滲漏,盡管小鼠不表達人類ACE2受體,也不會感染SARS-CoV-2。
最后,在RNA測序的幫助下,研究人員發現刺突蛋白通過一個涉及聚糖、整合素和轉化生長因子β (TGF- β)的分子信號通路觸發血管泄漏。通過阻斷整合素的活性,該團隊能夠逆轉小鼠的血管泄漏。
“我們發現了SARS-CoV-2的一種新的致病機制,其中刺突蛋白可以打破我們血管系統的屏障。由此導致的通透性增加會導致血管滲漏,就像在嚴重的COVID-19病例中經常觀察到的那樣,我們可以在我們的小鼠模型中重現這些疾病的表現,”研究合著者、加州大學伯克利分校公共衛生學院Harris實驗室的研究生Felix Pahmeier說。“看到刺突病毒蛋白和登革病毒蛋白NS1之間的異同是很有趣的。兩者都能破壞內皮屏障,但兩者之間的時間線和宿主途徑似乎不同。”
雖然阻斷整合素的活性可能是治療嚴重COVID-19的一個有希望的靶點,但Harris說,需要做更多的工作來了解這一途徑在疾病進展中的確切作用。雖然血管通透性增加會加速感染并導致內出血,但它也可以通過讓免疫機制更好地接近被感染的細胞來幫助身體對抗病毒。
“SARS-CoV-2進化出一種刺突表面蛋白,通過獲得RGD motif,與宿主細胞膜因子(如整合素)相互作用的能力增強。該motif是一種常見的整合素結合因子,被許多病原體利用,包括細菌和其他病毒,來感染宿主細胞,”Harris實驗室的前助理項目科學家、該研究的共同第一作者Francielle Tramontini Gomes de Sousa說。“我們的研究顯示了峰值RGD如何與整合素相互作用,導致TGF- β釋放和TGF- β信號的激活。利用上皮細胞、內皮細胞和血管通透性的體外和體內模型,我們能夠更好地了解COVID-19患者TGF- β水平升高的細胞機制,以及spike-宿主細胞相互作用如何導致疾病。”
該團隊正在繼續研究導致血管泄漏的分子機制,并正在研究其他導致人類嚴重疾病的病毒中可能的病毒毒素。
“COVID-19沒有消失。我們現在有更好的疫苗,但我們不知道病毒未來會如何變異。研究這一過程可能有助于我們開發一種新的藥物庫,這樣如果有人經歷血管泄漏,我們就可以針對它。也許它不能阻止病毒復制,但它可以阻止那個人死亡。”
Scott B. Biering, Francielle Tramontini Gomes de Sousa, Laurentia V. Tjang, Felix Pahmeier, Chi Zhu, Richard Ruan, Sophie F. Blanc, Trishna S. Patel, Caroline M. Worthington, Dustin R. Glasner, Bryan Castillo-Rojas, Venice Servellita, Nicholas T. N. Lo, Marcus P. Wong, Colin M. Warnes, Daniel R. Sandoval, Thomas Mandel Clausen, Yale A. Santos, Douglas M. Fox, Victoria Ortega, Anders M. Näär, Ralph S. Baric, Sarah A. Stanley, Hector C. Aguilar, Jeffrey D. Esko, Charles Y. Chiu, John E. Pak, P. Robert Beatty, Eva Harris. SARS-CoV-2 Spike triggers barrier dysfunction and vascular leak via integrins and TGF-β signaling. Nature Communications, 2022; 13 (1) DOI: 10.1038/s41467-022-34910-5

- 上一篇
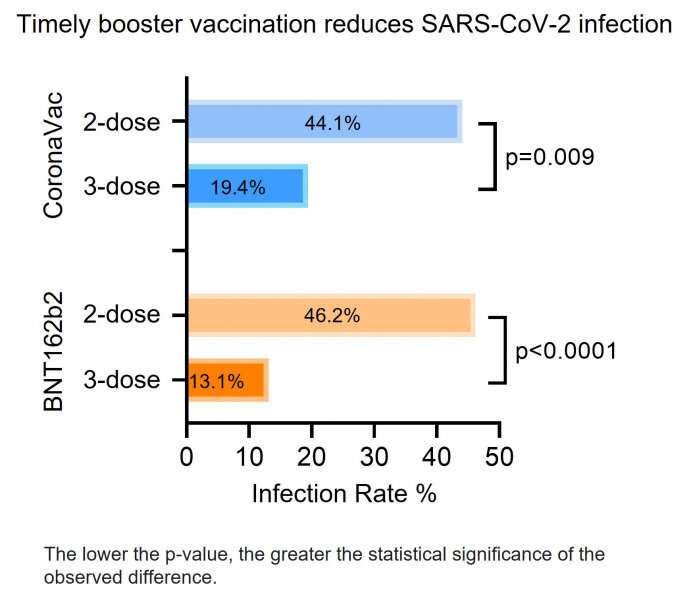
香港大學:及時加強疫苗接種可減少omicron突破感染和COVID-19嚴重程度
資料來源:香港大學香港大學臨床醫學院微生物學系艾滋病研究所和新發傳染病國家重點實驗室的研究人員發現,及時接種冠狀病毒疫苗或BNT162b2疫苗對誘導激活病毒特異性記憶B細胞和omicron交叉反應T細胞反應至關重要,從而顯著降低突破性感染的頻率和疾病嚴重程度。在接受過三劑疫苗的人群中,BA.2.12.1和BA.4/5的中和抗體效
- 下一篇
《NEJM》中國臨床試驗表明,新型冠狀病毒藥物可能優于Paxlovid
COVID-19患者很快就可以服用一種新的抗病毒藥物來預防嚴重疾病。在中國進行的一項三期臨床試驗中,這種名為VV116的治療方法與Paxlovid一樣,對患有嚴重疾病的高風險人群有效。該研究的合著者、上海交通大學醫學院教授Ren Zhao在宣布結果的新聞發布會上說,試驗取得了“巨大成功”。與抗病毒輸液瑞德西韋(remdesivir)
